Wasserhärte mit unterschiedlichen Bezeichnungen
Wir haben im SBZ Monteur bereits berichtet über die Auswirkungen von Wasserhärte und über Gegenmaßnahmen. Eine Frage wird jedoch immer wieder aufgeworfen und die dreht sich um ein Detail in diesem Zusammenhang, nämlich um die zahlenmäßige Einordnung.

Grundsätzlich sind die Härtebildner in den meisten Wässern die ins Haus geliefert werden vorhanden. Als Füll- und Ergänzungswasser wird es dann beispielsweise in die Heizungsanlagen gefüllt. Dort wird dann abhängig von der Härte des Wassers auf Dauer eine Kalkschicht gebildet, die einen effizienten Wärmeübergang behindern kann. Je nach Dicke dieser Isolierschicht erhöht sich daher die Abgastemperatur. Das bedeutet dann einen Mehrverbrauch an fossilen Brennstoffen. Wir, als Anlagenmechaniker, müssen gegenlenken der Umwelt und Wirtschaftlichkeit zuliebe. Welche Maßnahmen vorgeschrieben werden hängt natürlich von der Härte des Füll- und Ergänzungswasser ab. Auch der Gebrauch von Trinkwasser kann durch extreme Wasserhärte beeinträchtigt werden, denn Armaturen und Wärmetauscher vertragen den Kalkausfall auch nur in Maßen.
Ob ein Wasser als hart oder weich kategorisiert wird, kann anhand von Zahlen festgelegt werden, die wir hier erläutern.

Alte Bezeichnung
Ein recht einfaches und plausibles Verfahren der Benennung hatte man sich in Deutschland ausgedacht. Befindet sich also in einem Liter Wasser 10 Milligramm des Härtebildners Calciumoxid, gemäß Periodensystem der Elemente (PSE) mit -CaO- abgekürzt, dann entspricht dies ein Grad deutscher Härte abgekürzt 1 °dH. Ein weiterer Härtebildner, nämlich das Salz des Magnesiums, also Magnesiumoxid mit dem Kürzel -MgO- im PSE fand eine andere Wertigkeit. Die Masse von 7,19 mg MgO in einem Liter Wasser wurde ebenfalls mit 1 °dH angenommen. Das Salz des Calciums und des Magnesiums wird also als Masse in einem Wasservolumen für die Bewertung der Härte herangezogen. Das ist logisch, reichte aber nicht um dem SI-Maßsystem gerecht zu werden. SI steht für Système international d’unités. Weltweit legt man also Wert auf ein einheitliches System der physikalischen Einheiten. Man will damit dem Wirrwarr an unterschiedlichen Namensgebungen für ein und denselben Sachverhalt ein Ende bereiten und so zumindest bei physikalischen Größen eine einheitliche Sprache sprechen.
Historisch hatte beispielsweise die Elle mal eine Bedeutung als Längenmaß und entsprach dem Abstand zwischen Ellbogen und Mittelfingerspitze eines ausgewachsenen Mannes. Sie merken schon an diesem uralten Beispiel, dass man nicht ordentlich Handel treiben kann, wenn man eine Stoffbahn mit einer Breite von einer Elle und einer Länge von 50 Ellen bestellt. Das Interesse von Verkäufer und Käufer den entsprechenden ausgewachsenen Mann zur Längenbestimmung heranzuziehen ist doch sehr unterschiedlich.
Also, wie wird die Härte von Wasser zurzeit SI-gerecht benannt?

SI-Einheit für Härte
Vorweg schon mal, man drückt die Härte von Wasser in Millimol pro Liter aus, abgekürzt mmol/l. Dahinter steckt aber nicht etwa eine abstrakte oder gar unverständliche Größe. Sie ist einfach verständlich, wenn man die Zusammenhänge kennt. Die Kenntnis bringt aber den Durchblick für vielerlei Beziehungen in der Chemie. Das Thema Wasserhärte und auch die Verbrennungslehre lassen sich besser nachvollziehen, wenn man den Umgang mit Mol als SI-Einheit einmal begriffen hat. Ein einfaches Beispiel zeigt auf, was da gegenübergestellt wird.
Vergleich mit Dutzend
Im Titelbild zu diesem Bericht sehen Sie einen Messbecher mit 1 Liter Wasser und einem Dutzend Spax-Schrauben. Das Dutzend ist uns im deutschen Sprachraum geläufig und bezeichnet die Zahl zwölf.
Die Chemiker dieser Welt haben sich auf einen anderen Zahlenwert geeinigt der diesen Leuten vorteilhaft erschien. Nicht zwölf sondern 602 Trilliarden Teilchen werden als 1 Mol zusammengefasst.
Etwas genauer sind das
6,02214129 • 1023 Teilchen.
Diese Zahl ist als Avogadro-Konstante eingeführt.
Wenn also in einem Liter Wasser rund 6 mal 1023 Teilchen CaO vorhanden sind, spricht man von 1 Mol CaO pro Liter Wasser.
Wenn im SBZ Monteur ein Messbecher mit 12 Spax-Schrauben abgebildet ist, sind das 1 Dutzend pro Liter.
Ein Dutzend oder 1 Mol ist also nur eine Wortschöpfung um eine Anzahl abgekürzt bezeichnen zu können.
Die Chemiker dieser Welt wissen also etwas mit dieser Bezeichnung anzufangen.
Da das Lösevermögen für CaO jedoch geringer ist als 1 Mol pro Liter setzte man in der Bezeichnung noch ein Milli voran. Es ist also nur der Tausendste Teil eines Mols den man in diesem Fall sinnvoll beschreiben möchte. Da sind dann lediglich rund 6 • 1020 CaO in einem Liter
Ausgeschrieben wird also die Härte von Wasser in
Millimol pro Liter
ausgegeben.
Die Einheit selbst wird in
mmol / l
dargestellt
Spaßeshalber könnte man die Zahl 1,2 auch als Dezidutzend bezeichnen, macht aber keiner.
Was damit anfangen?
Natürlich werden wir Anlagenmechaniker nur sehr selten abdriften und als Chemiker eine Karriere starten. Aber die Kenntnisse hieraus nehmen dem Wert für Wasserhärte den wissenschaftlichen Geruch. Es geht nun mal „nur“ um die Anteile an CaO und anderen Härtebildnern im Wasser.
Außerdem hat man die Chance zu verstehen, warum beispielsweise verschiedene Umrechnungen zu einem bestimmten Härtegrad von Wasser beitragen.
Zur Härte von Wasser tragen, wie eingangs beschrieben die Salze des Calciums und des Magnesiums bei. Um den Härtegrad zu bestimmen kann man anhand einer Wasseranalyse folgende Beziehung aufstellen:
[Ca-Wert in mg/l] / 40
+
[Mg-Wert in mg/l] / 24,3
= Härtegrad des Wassers in mmol/l
Ein Beispiel verdeutlicht die Anwendung der Formel:
Die Trinkwasseranalyse eines Versorgers weist den Anteil an Calcium mit 72 mg/l und den Anteil von Magnesium mit 4,4 mg/l. Wie hoch ist die Härte in mmol / l?
72 / 40 + 4,4 / 24,3 = 1,98
Aber warum teilt man beim Calcium durch 40 und beim Magnesium durch 24,3?
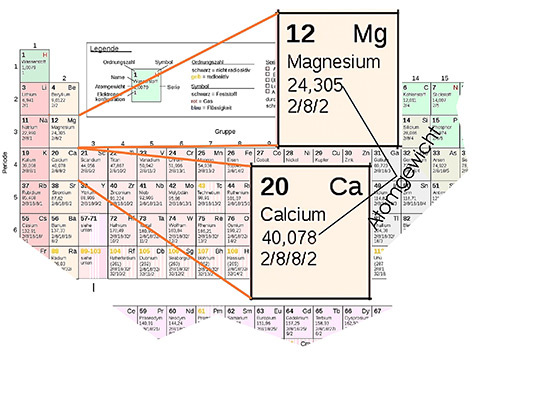
Die Antwort dazu findet man im PSE. Da werden sämtliche Elemente aufgeführt und eine dem jeweiligen Element zugeordnete Zahl benennt das Atomgewicht. Auch das hört sich sehr theoretisch, meint aber wieder etwas ganz banales, wie Sie gleich erkennen können.
Ein Dutzend Spax-Schrauben 4 x 300 mm wiegen zusammen 20 Gramm
Eine Größeneinheit könnte also sein
20 Gramm / Dutzend
In Anlehnung an diese erfundene Größeneinheit Gramm / Dutzend hat man im PSE auch die Werte hinterlegt für, Sie ahnen es schon, 1 Mol eines Stoffes, also 6 mal 1023 Teilchen. Und 1 Mol Calcium wiegt nun mal 40 Gramm, ein Mol Magnesium 24,3 Gramm.
Man setzt also für die Stoffmengen den unter Chemikern bekannten Wert für Mol ins Verhältnis zum Gewicht, um die Härte des Wassers zu bestimmen.
Ein weiteres Beispiel nimmt den letzten Schrecken vor diesen Beziehungen.
In einem Liter Wasser sind nach einer gründlichen Messung 40 Gramm Spax-Schrauben der Größe 4 x 300 enthalten. Wie viele Dutzend sind das pro Liter Wasser?
40 g / 20 (g/Dutzend) = 2 Dutzend
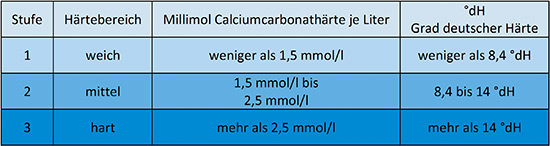
Umrechnungen allgemein
Die in Deutschland immer noch gebräuchliche Einheit für die Härte des Wassers bezieht sich auf CaO beziehungsweise auf MgO. Die Wasseranalyse eines Versorgers weist aber in der Regel den Anteil an Ca und Mg in Milligramm pro Liter aus. Das zusätzliche Gewicht von Sauerstoff [O] beim CaO und MgO wird also rausgerechnet für die Bestimmung der Härte.
Es bleiben daher letztlich zwei reduzierte Formeln über um aus der Wasseranalyse eines Versorgers die Härte zu bestimmen:
Ergebnis gesucht in mmol/l:
[Ca-Wert in mg/l] / 40
+
[Mg-Wert in mg/l] / 24,3
Ergebnis gesucht in °dH
0,14 • [Ca-Wert in mg/l]
+
0,23 • [Mg-Wert in mg/l]






